NMN 全球合规化破冰!Uthever® 领跑欧盟Novel Food认证
2025年03月04日 | 音芙小艾
全球抗衰合规化进程迎来里程碑
2025年2月底,音芙医药旗下核心原料Uthever® NMN在欧盟新食品原料(Novel Food)认证中率先完成公众咨询阶段,成为全球首个进入欧洲食品安全局(EFSA)最终审查的NMN产品,有望在2025年年内通过Novel Food认证,成为全球范围内首个获欧盟新食品原料认证的NMN原料。这一进展标志着NMN即将迎来“迈向全球主流合规”的关键转折。若最终获批,Uthever® NMN将解锁欧盟28国食品与膳食补充剂市场,撬动全球50亿美元的抗衰市场[1]。
01监管破冰:欧盟Novel Food认证的战略价值
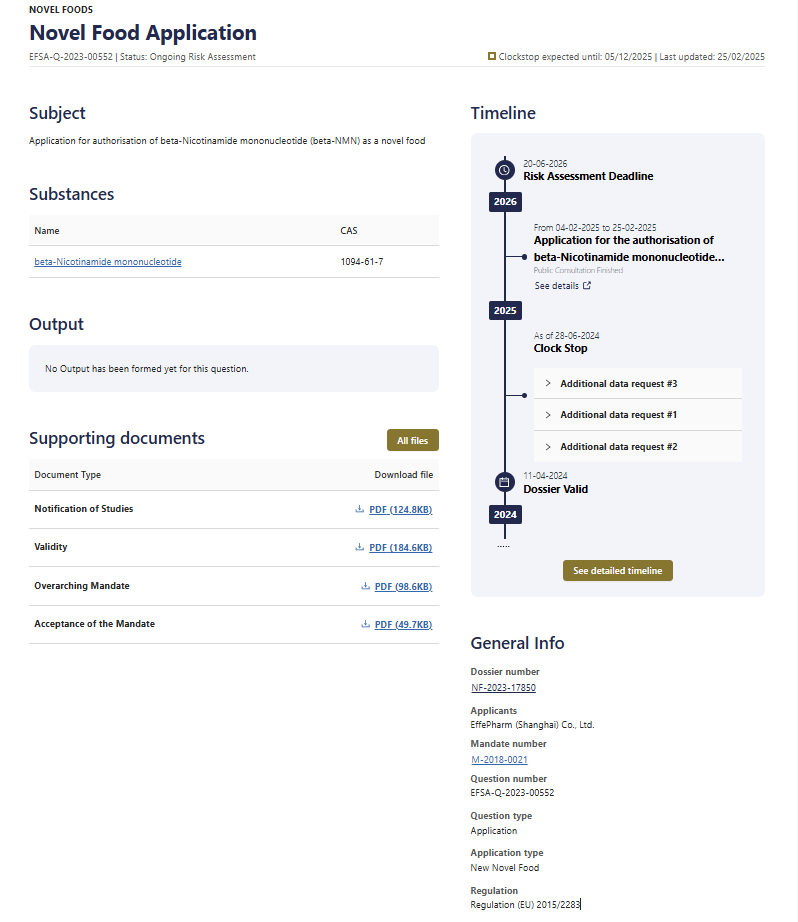
欧盟Novel Food认证作为NMN等尖端抗衰原料合规化的“黄金通路”,以全链条科学审查体系构建了严苛的技术壁垒。申请主体需提交涵盖毒理学(90天动物试验)、代谢动力学(ADME)及稳定性数据的完整档案,2023年EFSA(欧洲食品安全局)统计显示其综合通过率不足30%。
| 阶段 | Uthever® NMN |
| 申请提交 | 2023.08 |
| EFSA风险评估 | 2024.04 已启动 |
| 公众咨询 | 2025.02 已完成 |
Uthever® NMN凭借其卓越的产品质量和严格的安全标准,提前布局欧盟Novel Food安全认证:2025年2月通过公众咨询阶段,当前进度较同类企业提前3-6个月,预计于2025年6月完成风险评估,有望年内获Novel Food安全性认证。
02 技术制胜:以临床实证引领技术创新
Uthever® NMN是全球首个进行大规模人体临床研究的NMN原料品牌。音芙坚持临床实证,通过规范的毒性测试与人体功效验证流程,系统性论证原料的生物安全性与生理活性。
针对“Uthever® NMN”与“UthPeak® NMNH”两大核心抗衰老成分,研究设计严格遵循国际通行的科研伦理标准,覆盖多年龄段人群样本,建立从体外实验到人体观察的递进式验证机制,形成符合行业规范的证据链条,为产品应用提供科学支撑。

03 市场重构:临床实证NMN引领科学抗衰新纪元
欧盟合规认证体系为Uthever® NMN构建了从跨境贸易、线上渠道向主流零售跃迁的战略通道。通过获得欧洲市场准入资质,该原料得以整合进入Boots、Sephora药妆专柜及Carrefour Bio等实体零售网络,实现渠道结构从“线上专供”向“双轨并行”的升级。这种转型将直接拉动销量增长——实体渠道触达的中高端健康消费群体与跨境电商既有流量形成叠加效应,进一步放大Uthever® NMN的品牌价值与知名度效应,打开欧洲抗衰市场新空间,并带动全球分销网络升级与法规落地,最终撬动全球50亿美元的抗衰市场。
从中国智造,到全球健康话语权
“欧盟认证不是终点,而是中国智造定义抗衰产业规则的起点。”音芙医药以临床实证创新为支点,正在重构全球抗衰老产业的价值链。通过核心技术专利布局与国际法规申报体系的双轨协同,音芙不仅完成从“中国制造”向“标准输出”的跨越,更在欧盟市场验证了中国尖端抗衰科技的产业话语权。其构建的“研发-认证-量产”闭环体系,已形成可复制的技术转化模式,为全球抗衰原料市场注入新动能。
- 上一篇: 时光淬炼,科技护航:妳的每段年华都是黄金时代
- 下一篇: 🎊🐍 音芙与您携手,恭贺新春!🐍🎊
本网站为音芙医药科技(上海)有限公司的官方中文站点。特此声明,本网站所展示的部分产品可能尚未获得中国境内的销售许可,因此并不在中国市场进行销售。用户在使用本网站信息时,请自行判断信息的适用性,并遵守所在国家或地区的法律法规。

